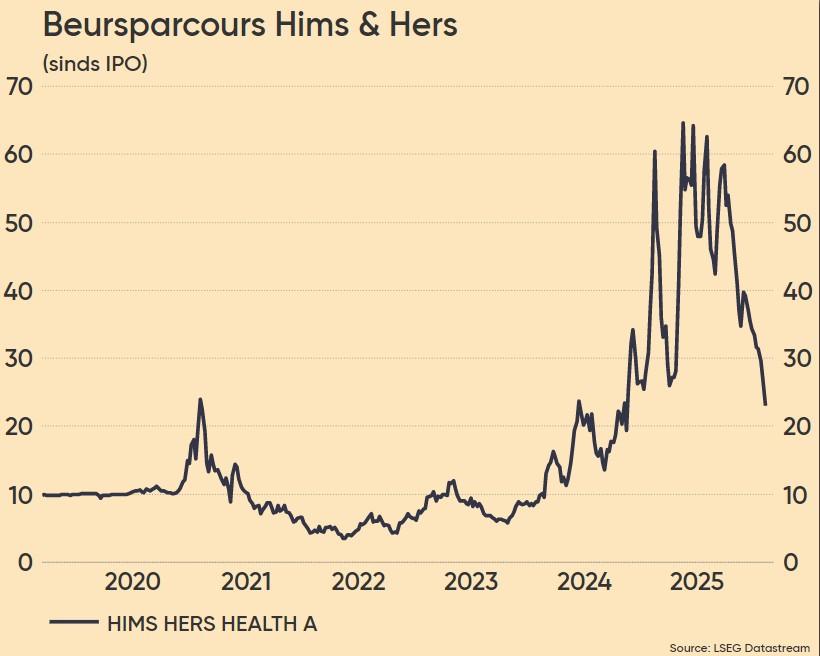
Hims & hers opnieuw over de GLP-1-schreef
Uit het departement: “Dat het sloebers zijn”

De plotselinge stap van Hims and hers om een samengestelde orale semaglutidepil op de markt te brengen voor slechts 49 dollar heeft een schokgolf door de wereld van medicijnen tegen obesitas gestuurd. Voor de grote spelers zoals Novo Nordisk, Eli Lilly en de hele biofarmaceutische sector is het idee dat een telegezondheidsplatform FDA-goedkeuringen en gevestigde IP-beschermingen kan omzeilen, zeer verontrustend. Als deze benadering standhoudt, ontstaat het vooruitzicht dat elk merkgeneesmiddel kan worden nagemaakt onder de brede paraplu van “magistrale bereidingen”.
Verspilling
Toen het nieuws bekend werd, wees de CEO van Novo Nordisk - die sprak op een analistenbijeenkomst in Londen - er snel op dat hun orale semaglutide beschermd wordt door formuleringsoctrooien tot ver in de jaren 2030. Ze benadrukten dat het medicijn simpelweg niet kan worden opgenomen zonder hun SNAC-technologie, die ervoor zorgt dat semaglutide het spijsverteringsstelsel kan overleven. Ondertussen doet Hims slechts vage beweringen over een "innovatieve toedieningsmethode" die de absorptie beschermt, zonder technische details te verstrekken. De CEO van Novo deed het hele product af als een verspilling van 49 dollar en merkte ook op dat de prijs na de introductieperiode stijgt naar 99 dollar
De visie van KBC Asset Management
Eén en ander roept onmiddellijk wetenschappelijke en juridische vragen op. Heeft Hims effectief een generische versie geïntroduceerd van een volledig gepatenteerd geneesmiddel waar geen tekort aan is? Als dat zo is, kan het bedrijf mogelijk ernstig aansprakelijk worden gesteld voor inbreuk. En als hun pil geen echte kopie is, is er geen bewijs dat het werkt - geen farmacokinetische gegevens, geen wettelijke evaluatie en geen duidelijkheid over de veiligheid, en toch zou het in de handen van miljoenen mensen terecht kunnen komen.
Dit alles leidt terug naar het grijze gebied dat is gecreëerd door de 503A wet voor magistrale bereidingen, die apotheken toestaat om patiëntspecifieke medicijnen te maken zonder goedkeuring van de FDA of volledige naleving van Good Manufacturing Practices. Bereidingsapotheken hebben deze grenzen al verlegd met injecteerbare GLP-1 alternatieven en signalen van regelgevende instanties vorig jaar suggereerden dat de deur al op een kier stond. Hims zet die deur nu wagenwijd open.
Op dit moment vraagt de situatie om een gecoördineerde reactie van de industrie. Zonder krachtigere regelgeving dreigt het huidige vacuüm het hele kader te ondermijnen dat de goedkeuring van medicijnen, veiligheid en intellectueel eigendom regelt. De status quo is gewoon niet houdbaar.
FDA schoot dit weekend in actie
Sinds vrijdag heeft de situatie een dramatische wending genomen. De FDA heeft eindelijk duidelijk actie genomen tegen telehealth‑bedrijven die ongekeurde, samengestelde GLP‑1‑middelen massaal verkopen, waarbij Hims & Hers expliciet werd genoemd. De toezichthouder nam alvast deze beslissingen.
- Toegang tot GLP‑1‑ingrediënten wordt beperkt: De FDA heeft bevestigd dat zij de toegang tot actieve GLP‑1‑ingrediënten voor niet‑goedgekeurde samenstellingen gaat beperken, vanwege zorgen over kwaliteit, veiligheid en mogelijke wettelijke overtredingen.
- Ticketje richting Ministerie van Justitie: Het Department of Health and Human Services heeft Hims & Hers officieel doorverwezen voor federale vervolging wegens mogelijke schendingen van de Federal Food, Drug, and Cosmetic Act.
- Expliete FDA‑waarschuwing tegen de massaverspreiding van “illegale copycat drugs”: FDA‑commissaris Marty Makary liet via Twitter weten dat de FDA snel zal optreden tegen bedrijven die illegale copycat‑versies van FDA‑goedgekeurde medicijnen massaal op de markt brengen.
Het rechtstreekse gevolg liet niet lang op zich wachten. Hims & Hers benadrukte dat het “constructieve gesprekken” heeft gevoerd en de behandeling per direct van het platform haalt. Einde verkoop, dus, van de samengestelde semaglutidepil én de lijn wordt volledig geschrapt.
Pijnlijk, amper twee dagen na de lancering ervan. De FDA gebruikte die beslissing om nog eens aan te geven dat samengestelde GLP‑1‑producten niet als generiek of equivalent aan goedgekeurde middelen mogen worden gepositioneerd. Dit sluit nauw aan bij eerdere waarschuwingen richting de sector en dat kan dus (eindelijk) een precedent scheppen dat mass‑compounding voor GLP‑1‑injecties effectief beëindigt, nu er geen officieel tekort meer is.