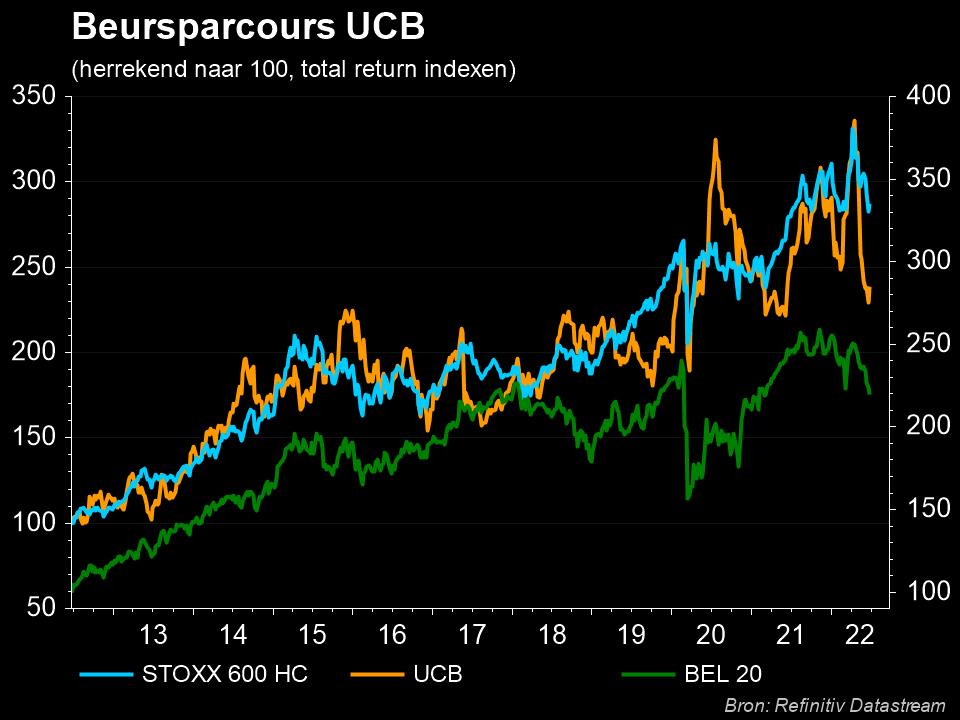
Lawine van goed nieuws bij UCB
Uit het departement: “Op naar een All Time High beurskoers”

UCB meldde een lawine van goed nieuws over Bimzelx en Fintepla. De FDA heeft Fintepla (fenfluramine) goedgekeurd voor de behandeling van aanvallen die gepaard gaan met het Lennox-Gastaut-syndroom. Bovendien werden er dit weekend niet minder dan 11 abstracts gepubliceerd die de langetermijnprestaties aantonen van haar IL17 A/F-remmer Bimzelx voor de behandeling van matige tot ernstige plaque psoriasis. Dat is allemaal positief volgens KBCS, dat het “Kopen”-advies en 125 euro koersdoel daarom maar wat graag in de verf zet.
Fintepla For The Win
De Amerikaanse geneesmiddelenwaakhond FDA heeft Fintepla (fenfluramine) goedgekeurd voor de behandeling van epilepsie aanvallen die gepaard gaan met het Lennox-Gastaut-syndroom (LGS) bij patiënten van twee jaar en ouder. De goedkeuring werd ondersteund door veiligheids- en doeltreffendheidsgegevens van een wereldwijde, gerandomiseerde, placebogecontroleerde klinische studie van fase 3 bij 263 patiënten met LGS, die een leeftijd hadden tussen 2 en 35 jaar. De studie toonde aan dat fenfluramine in een dosis van 0,7/mg/kg/dag de frequentie van druppelaanvallen aanzienlijk verminderde in vergelijking met een placebo (p=0,0037).
De lancering van een nieuw geneesmiddel is een complexe onderneming, waar op vele fronten tegelijk moet worden gevochten. In een zeer competitieve omgeving zoals psoriasis is het daarenboven nog eens extra moeilijk om artsen en betalers te overtuigen om een nieuw middel te aanvaarden. De klinische gegevens zijn uiteindelijk het krachtigste instrument voor de verkoop. UCB lijkt een prachtige klinische symfonie te voeren rond zijn toekomstige gouden gans Bimzelx, waarbij wordt gekeken naar de langetermijnprestaties van het geneesmiddel en hoe het presteert in vergelijking met de concurrenten. Dit laatste zal van cruciaal belang zijn, aangezien de concurrenten niet bepaald onbelangrijke spelers zijn in de farmaceutische wereld en onder meer Abbvie (Humira), J&J (Stelara) en Novartis (Cosentyx) omvatten. Deze laatste is sinds 2015 de nummer 1 voorgeschreven IL-17A-remmer voor alle indicaties bij volwassenen en bijna 200.000 patiënten krijgen het geneesmiddel voorgeschreven in de VS.
Het is belangrijk om te begrijpen dat de studies uitgevoerd door UCB head-to-head waren, en geen post-hoc vergelijkingen tussen verschillende trials die de zaken zouden hebben gecompliceerd (aangezien er andere factoren zijn die de klinische uitkomst kunnen beïnvloeden). De BE RADIANT studie toonde reeds aan dat Bimzelx sneller werkt dan Cosentyx (71% vs. 47,3% van de patiënten bereikte PASI75 na 4 weken). Uit deze gegevens blijkt dat het overschakelen van patiënten die niet reageren op Cosentyx naar Bimzelx leidt tot betere klinische resultaten (in bijna 80% van de gevallen), en dat als zij reageren op Cosentyx, het overschakelen op Bimzelx geen effect heeft op de klinische resultaten.
Bovendien blijkt uit andere gegevens dat Bimzelx weliswaar snel werkt, maar ook gedurende langere perioden (in deze studies tot 2 jaar) goede klinische resultaten blijft opleveren voor patiënten. De algemene conclusie lijkt daarom te zijn dat artsen die patiënten met psoriasis Bimzelx geven, het geneesmiddel niet zullen hoeven te vervangen en dat Bimzelx een zeer goed alternatief zal zijn voor patiënten die niet reageren op Cosentyx.
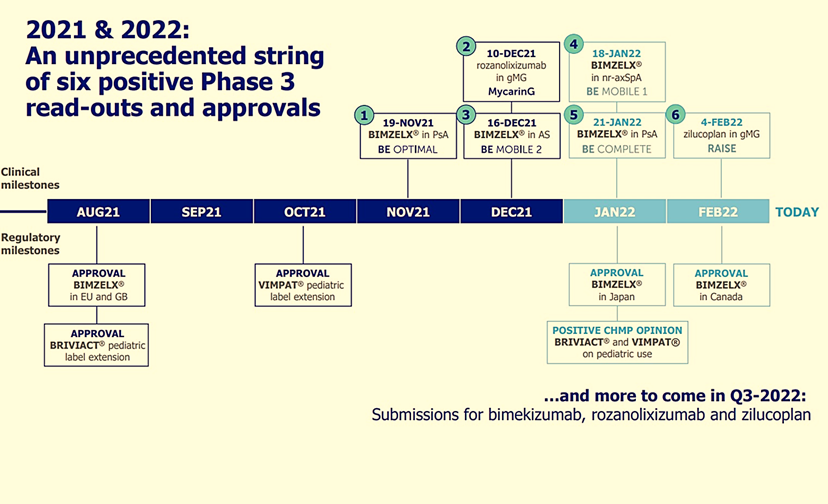
Bimzelx blijkt nog nuttiger dan gedacht
Er werden dit weekend ook niet minder dan 11 abstracts gepubliceerd op de jaarvergadering van de American Academy of Dermatology (AAD) van 2022. Die tonen de langetermijnprestaties aan van haar IL17 A/F-remmer bimekuzimab (onder de commerciële naam Bimzelx) voor de behandeling van matige tot ernstige plaque psoriasis bij de behandeling van volwassenen met matige tot ernstige plaque psoriasis.
De gegevens toonden aan dat meer dan 80% van de patiënten die volledige huidklaring (PASI100) bereikten op week 16 en deelnamen aan de open-label extension (OLE) studies, deze respons behielden gedurende de opvolgperiode in de twee daaropvolgende jaren. Er werden daarenboven geen nieuwe veiligheidssignalen geïdentificeerd. Bovendien bleven de klinische responsen (PASI100 en absolute PASI, PASI <2) die werden bereikt op week 48 behouden tot week 96 met voortdurende behandeling met bimekizumab en verbeterden ze voor patiënten die van secukinumab (Cosentyx) overstapten op bimekizumab bij deelname in de proef.
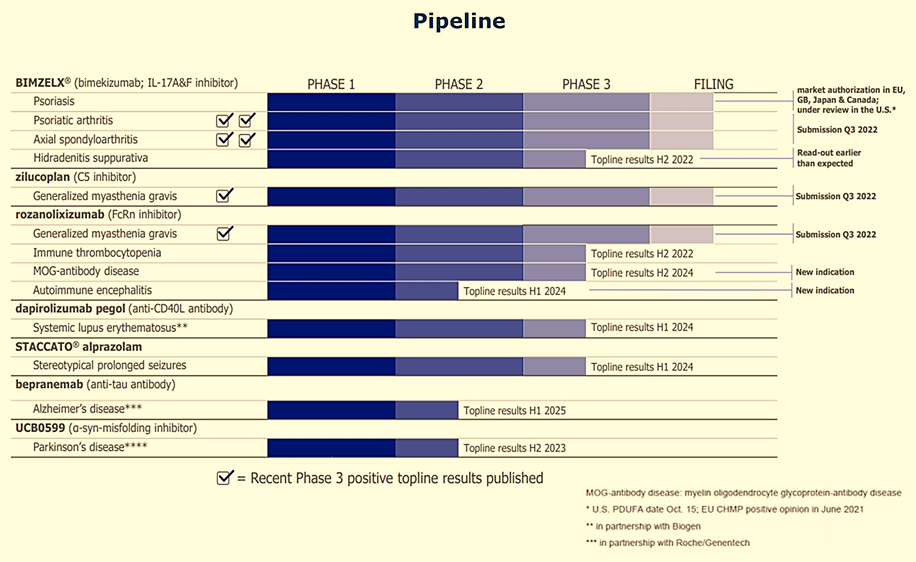
De mening van KBC Securities
Het was duidelijk een sterk weekend voor UCB, dankzij positief nieuws over Bimzelx en de FDA-goedkeuring voor Fintepla. Het latere nieuws toont aan dat de overname van Zogenix op het juiste moment kwam en een zeer sterke strategische zet was van UCB.
De FDA heeft Fintepla nu goedgekeurd voor 2 indicaties, zowel voor het syndroom van Dravet als voor LGS. Hoewel voor Dravet de vergelijking met concurrent Epidiolex (cannabidiol) meer uitgesproken was, hebben patiënten met epileptische aandoeningen, vooral bij LGS, niet veel opties en moeten artsen op zoek naar een therapieregime dat werkt. KBC Securities merkt op dat dankzij de opzet van de klinische studie die Zogenix heeft uitgevoerd, dit heeft geresulteerd in pediatrische exclusiviteit voor Fintepla in LGS. Dit is een zeer ernstige en zeldzame vorm van epilepsie, die naar schatting 30.000 tot 50.000 patiënten treft in de VS. KBCS had al een 90% kans ingerekend voor goedkeuring in het waarderingsmodel.
Wat Bimzelx betreft, is het duidelijk dat UCB een zeer sterke klinische dataset over het product samenstelt. UCB positioneert het als beste in zijn klasse (vooral door de snelle werking), maar kijkt nu ook naar het langetermijnperspectief (+2 jaar). Wat de vergelijkende studie versus het IL17A-medicijn Cosentyx van Novartis betreft, lijkt het erop dat het overschakelen van niet-responderende patiënten van Cosentyx naar Bimzelx tot betere klinische resultaten leidt (in bijna 80% van de gevallen), en als ze op Cosentyx reageren, heeft het overschakelen op Bimzelx doorgaans geen invloed op de klinische resultaten. Als dusdanig is UCB zeer goed gepositioneerd om de “dynamische” markt van psoriatica aan te pakken. KBC Securities blijft optimistisch over UCB en herhaalt daarom met plezier het koersdoel van 125 euro en het “Kopen”-advies.